国内《化学药品注射剂灭菌和无菌工艺研究及验证指导原则(试行)》中是这样描述的:“湿热灭菌工艺的微生物挑战试验是指将一定量已知 DT值的耐热芽孢(生物指示剂)在设定的湿热灭菌条件下进行灭菌,以验证设定的灭菌工艺是否确实能使产品达到预定的无菌保证水平。生物指示剂被杀灭的程度,是评价一个灭菌程序有效性的直观指标。”但这个描述也过于泛泛。我们来看一下美国药典是怎么说的。USP1229在灭菌周期控制(sterilization cycle control) 段落中提到了FPHY (物理杀灭时间),说明了其是有电脑自动化系统监测所得的物理数据,将其进一步计算成灭菌过程的致死率(即FPHY ),并由此确定灭菌操作是否达到预定目的。USP主要是将FPHY 应用于确认灭菌过程是否符合预定,偏向于过程管控的概念,而对于灭菌方法的开发研究,或是评估灭菌方法的效果时,则较注重于微生物挑战的实验结果,也就是FBIO(生物杀灭时间)。FPHY 和FBIO 两者双管齐下一起支持灭菌方法开发或灭菌效果确认。USP1229还特别强调了FPHY 和FBIO 两者之间应具有合理的一致性。(The lethality-based PHYsical measurement and BIOlogical inactivation data from a sterilization process should be in reasonable agreement)
至于欧盟,在EP5.1.1中,强调计算所得的FPHY 应与FBIO具有相关(Calculated effectiveness from PHYsical parameters (FPHYs) is correlated with BIOlogical effectiveness (FBIO))。而在EMA《药品、活性物质、辅料和内包材灭菌指南-2019》中则强调灭菌效果以负载状态灭菌样品的FPHY 和FBIO作为评估指标,同样也指出FPHY 和FBIO具有相关性。
相较于美国和欧盟的法规,我国法规《化学药品注射剂灭菌和无菌工艺研究及验证指导原则(试行)》着重于具体的微生物挑战试验怎么做,直接推荐了生物指示剂的使用菌种,甚至专门列了一个附件2来专门介绍生物指示剂的芽孢数如何计算。但若无背景知识,根本就无法理解为什么要这样计算。我们继续查阅了注射剂协会(PDA)1号技术报告《湿热灭菌的验证:灭菌程序的设计、开发、确认和日常监控》,里面对灭菌科学有详尽的阐述。可以打个比方,PDA的技术报告是九阴真经的上卷,讲内功的;而各国的法规,药典等相关规定就是九阴真经的下卷,讲招式的。理解了PDA的技术报告,对各国法规就能有更加深刻的理解。
在恒定的热力灭菌条件下,同一种微生物的死亡遵循一级动力学规则,微生物死亡速率是微生物的耐热参数 D 和杀灭时间的函数,它与灭菌程序中微生物的数量无关。存活曲线可以用下面的半对数一级动力模式来表示:

公式中,F(T,z)——在规定的温度系数(z值)下,灭菌工艺期望获得的温度T/℃下的等效灭菌时间,min;
DT——微生物在温度T/℃下的耐热参数,min;
N0——灭菌前生物指示剂的初始芽孢数;
NF——灭菌后生物指示剂的存活芽孢数;
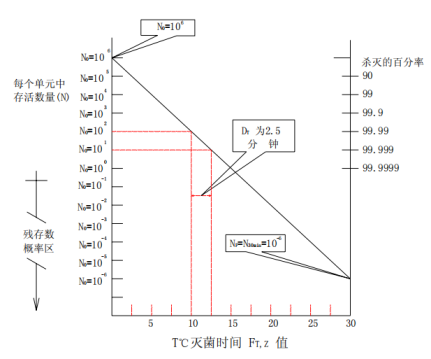
将上述公式进行变换,F(T,z)=(Lg N0-LgNF)×DT。一般而言,湿热灭菌的温度范围很窄,我们最多的选择是121℃,则Z值被看作一个常量10℃,DT为微生物在温度121℃下的耐热参数。当进行微生物挑战试验时,DT指生物指示剂所用菌种在121℃下的耐热参数,即D121℃。那么,FBIO(生物杀灭力)即可用公式FBIO=(Lg N0-LgNF)×D121℃来表示。这个公式的意义是表示生物指示剂系统测得的实际杀灭效果。
在具体操作时,将一定浓度和耐热性的湿热脂肪芽孢杆菌放置于灭菌系统各个代表性的位置,依据设定的灭菌程序进行灭菌,然后将生物指示剂取出做无菌检查。如所有指示剂均无存活孢子,则可均具灭菌前孢子数及D值计算FBIO,如灭菌后尚有孢子存活,则可将其培养、计数,再根据公式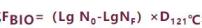 来计算FBIO值。
来计算FBIO值。
至于FPHY,是指以灭菌程序的物理参数计算的物理杀灭时间。121℃条件下灭菌1min,累计的FPHY为1。但由于灭菌柜中的温度会有一定的波动,而灭菌率也会相应波动。实际上FPHY值是整个灭菌程序中灭菌率的积分值,这个积分值是通过对梯形模式的数字累计而得:
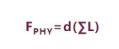
式中:
d=每次温度读数之间的间隔时间
L=经计算的各个温度下的灭菌率
在具体操作时,是将温度探头安装在灭菌柜内部各个有代表性的位置,运行灭菌程序,电脑自动化系统会监测到实时灭菌温度,并自动计算出累计的FPHY。
总的来说,FPHY(物理杀灭时间)是验证灭菌过程中的工艺参数,而FBIO(生物杀灭时间)则是验证灭菌过程产生的效果。和其他验证一样的思路,灭菌工艺验证也包含对参数和效果两方面的确认。
那么,具体应该如何设计微生物挑战试验呢?我们据几个例子。
例1 过度杀灭法(121℃、12min)的微生物挑战试验
对于过度杀灭的设计工艺,期望的物理杀灭时间 FPHY和生物杀灭时间 FBIO均大于或等于 12 分钟。如果选择使用耐热性为2.1分钟的生物指示剂,那么完全杀灭挑战试验中生物指示剂的最低(N0)可以通过以下方法计算得到:
LgN0 =LgNF+F/D
=Lg100+12/2.1
LgN0 =5.71
N0 =5.2×105
因此,能杀灭N0=5.2×105、D 值为2.1分钟的生物指示剂的灭菌程序,即是经生物指示剂确认的过度杀灭程序(FBIO≥12.0)。
注:为了方便计算,如果将生物指示剂杀灭,可以认为存活数小于1,在此等式中,可以 NF=100表示。
例2 残存概率法(121℃、8min)的微生物挑战试验
在实际操作中,可能并不容易找到一个适宜的生物指示剂,将其D值和孢子数计算后使得FBIO恰好刚刚大于8,而又不至于过高(残存概率法的FPHY<12,如果FBIO>则很有可能灭菌后生物指示剂中仍有芽孢存活)。但我们完全可以将一个确认试验设计成这样的终点,即没有必要将生物指示剂的芽孢完全杀灭。如果设计要求为FPHY=8 分钟;生物指示剂的起始数量(N0)为 2×106;D 值为 2.1 分钟,那么终点(NF)的最大值可以通过计算得到。
LgNF =LgN0-F/D
=Lg2×106-8.0/2.1
LgNF =6.3-3.8=2.50
NF =3.2×102
因此,如果灭菌程序 能使D值为2.1分钟的生物指示剂孢子数由N0=2×106降至 NF=3.2×102以下时,则证明生物杀灭时间FBIO≥8分钟,并且与物理杀灭时间FPHY等效。
例3 半周期法的微生物挑战试验
所谓半周期法,是在灭菌柜冷点的位置放置了初始细菌计数为106CFU的生物指示剂,其灭菌时间是所有生物指示剂死亡时间的两倍。在过度杀灭法中,灭菌时间为12min,而在半周期法中,灭菌时间为14min至16min。初始细菌计数为106CFU的生物指示剂的存活概率在7 min时为10%,在8 min时为1%,因此(7 min至8min)× 2=14min至16min。欧洲药典推荐的121℃,15min应该就是由此而来。
由于121℃,15min是个非常强力的灭菌条件,如果想直接验证FBIO≥15需要找到D值很高,孢子数很多的生物指示剂。但如果把前述半周期法的思路反过来,操作时将灭菌时间缩短一半(121℃,7.5min),那只要验证FBIO≥7.5就可以了。选择D为1.5分钟的生物指示剂最低灭活数可以通过以下方法计算:
LgN0 =LgNF+0.5×(F/D)
=Lg100+0.5×(15/1.5)
LgN0 =5
N0 =1.0×105
因此,如果采用半周期灭菌的确认方法,则须将D值为1.5、数量为1.0×105的生物指示剂杀灭,才能证明FBIO≥15分钟。