经验分享|巴西ANVISA医疗器械注册指南
按照巴西法律规定,医疗器械包含了一系列不同的产品,这些器械直接或者间接用于人类健康或者医疗服务,涉及医学、物理疗法、实验室诊断、康复、医疗、麻醉和健康监测等领域。
按照1976年9月23日颁布的6360法第12款,所有医疗器械均由卫生部管理,包括生产、使用,销售。巴西卫生监督管理局ANVISA 负责巴西医疗器械的注册,注册完成后,医疗器械都将有一个唯一的11位的注册码。
巴西所有电子设备都必须在INMETRO注册,注册完成后,取得INMETRO注册文件才能进行ANVISA医疗器械注册。巴西医疗器械注册根据难易程度分为常规注册和列出(或称简易注册)。
根据ANVISA规定,医疗器械根据风险等级,分类
一类 I 低风险、
二类II中等风险、
三类III高风险、
四类IV极高风险,
ANVISA收到的医疗器械信息后,评估风险,根据其风险等级决定其等级类别归属。
在ANVISA列出是所有医疗器械注册的第一步,也是一类和二类医疗器械的简易注册。根据1999年5月24日公布的RDA ANVISA, 大部分一类和二类医疗器械不需要进行RDA ANVISA注册,除非这些医疗器械可能对人体造成危害,则仍然需要注册。一类和 二类医疗器械也不需要关于有效性和安全性的研究,而且非医疗工作者也可以使用这些器械。
所有三类和四类医疗器械均须走列出和注册两个步骤,并且在注册时,需要提交所有的参数和指标,并且需要有临床试验来支持其安全性和有效性。
巴西ANVISA医疗器械注册审批流程图
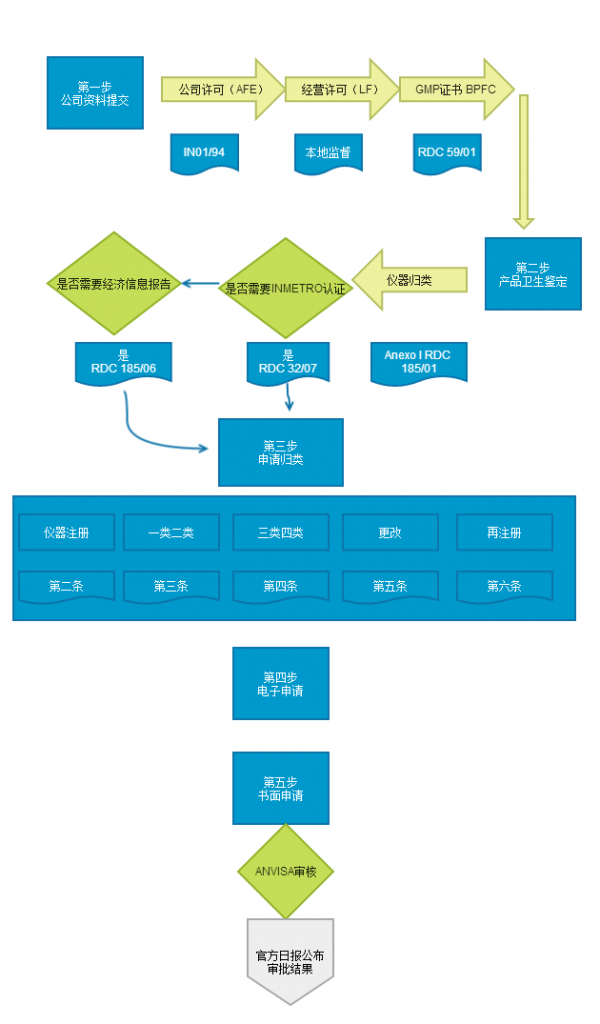
巴西ANVISA负责巴西医疗器械的审批和注册,上图为注册流程图
图中一些缩写的说明:
公司许可 Autorização de Funcionamento da Empresa – AFE
任何一个巴西公司都可以向ANVISA申请许可,外国公司须与巴西公司签署合作协议。
经营许可 Licença de Funcionamento local – LF
由所在城市或州政府的卫生部门颁发公司营运许可。
Boas Práticas de Fabricação e Controle – BPFC
巴西GMP证书,须符合2001年10月10日颁布的 3.961法案

全部 0条评论